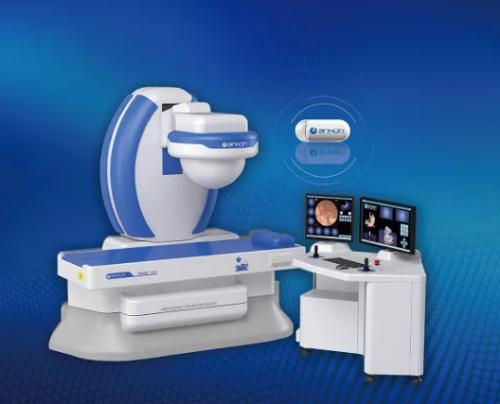
速递!安翰科技“磁控胶囊胃镜系统” 通过美国FDA注册
2020年5月下旬,安翰科技自主研发的NaviCam™“磁控胶囊胃镜系统”被美国食品和药物管理局(FDA)以De Novo创新医疗器械分类方式获批注册。
值得关注的是:安翰科技自主研发的NaviCam™“磁控胶囊胃镜系统”是美国FDA批准的第一个磁控胶囊内窥镜产品,也是中国胶囊内镜类医疗器械获批FDA的第一款产品。而之前,安翰科技自主研发的NaviCam™“磁控胶囊胃镜系统”已获得中国、欧洲相关认证,这次凭借美国FDA认可的创新医疗器械“独占鳌头”,获得美国FDA创新医疗器械注册证,意味着该技术对美国消化道检查医学技术进步意义重大。磁控胶囊胃镜系统获国际高度认可
美国食品药品监督管理局(U.S. Food and Drug Administration,缩写为FDA)为美国卫生与公众服务部直辖的联邦政府机构,在美国乃至全球都有极其巨大的影响,其信誉和专业水准深得诸多专家和各国的认同,其严格的检测和评估为药品和医疗器械的安全性提供了良好的保障。
De Novo分类方式适用于美国市场没有先例的的首次创新产品。2019年FDA仅批准了22个De Novo产品,很少有非美国本土研发产品获得De Novo批准。而安翰科技自主研发的的NaviCam™“磁控胶囊胃镜系统”能够顺利通过De Novo注册,其安全性、有效性、技术先进性和安翰的强大的研发实力不言而喻。
著名的UCLA加州大学洛杉矶分校David Geffen医学院临床医学教授Raman Muthusamy医学博士评价:"NaviCam™磁控胶囊胃镜系统为消化科医生提供了一种方便的、非侵入性的替代内窥镜检查的方法以获得胃内部的图像,提供有助于诊断患者症状的信息,磁力控制可以改善整个胃部的图像获取方式,并为那些对接受传统内镜检查犹豫不决的患者提供了一种新的选择。"
“NaviCam™磁控胶囊胃镜系统有可能成为一个有价值的工具来分类因上消化道原因的急诊患者,因为它可以快速可视化胃部从而达到更准确的急诊分流,”美国乔治华盛顿大学医院急诊医学主任Andrew Meltzer博士说。“此外,对于可能患有COVID-19等感染性疾病的患者,使用NaviCam™磁控胶囊胃镜系统可以使治疗医生在进行内镜检查的同时,减少其与患者的物理接触,这可能会使临床医生的感染风险降低。
填补美国FDA空白 实现胶囊内镜领域应用的新突破
第一代胶囊内镜只能查小肠不能精准查胃,属于被动式检查,不受控制。众所周知,胃部是一个空腔,因而要想实现对胃部的全面检查,达到传统电子胃镜的检查准确性,就必须要求胶囊内镜自始至终能够按照医生指示,精准而全面的游走于胃内各个角落,仔细拍摄沿途“风光”,反复观察疑似病灶并获取充足的医学影像,为后期诊断提供充分依据。
应该说,胶囊胃镜是人们最期望实现的梦想之一。减轻插管胃镜的痛苦,是医生、患者的共同期望。
然而,这一步跨越异常艰巨。原因是:可精准控制的胶囊胃镜,其研发难度很高。期间,各大跨国医疗器械公司均纷纷投入大量研发力量,但手持磁铁控制、核磁共振控制等技术方案均最终均没有实现商业化。
2013年,安翰科技自主研发的安翰“磁控胶囊胃镜系统”组成产品巡航胶囊内窥镜控制系统、定位胶囊内窥镜系统在分别获得原湖北省食品药品监督管理局(现为湖北省药品监督管理局)二类医疗器械注册证和原国家食品药品监督管理局(现为国家药品监督管理局)三类医疗器械注册证后,正式面世,并于2014年8月15日取得欧盟CE认证。
2020年5月,安翰“磁控胶囊胃镜系统”通过FDA De Novo及510K医疗器械注册,填补了胶囊内镜应用于全消化道检查最重要的空白——胃部检查。至此,胶囊内镜全面覆盖人体消化道检查,安翰科技为世界打开了消化道舒适化内镜检查的新篇章。
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。
“特别声明:以上作品内容(包括在内的视频、图片或音频)为凤凰网旗下自媒体平台“大风号”用户上传并发布,本平台仅提供信息存储空间服务。
Notice: The content above (including the videos, pictures and audios if any) is uploaded and posted by the user of Dafeng Hao, which is a social media platform and merely provides information storage space services.”